“Dentro de una década, esperamos aumentar la fertilidad entre las mujeres mayores que usan medicamentos antivirales”, dijo el Dr. Michael Klutstein, de la Universidad Hebrea.
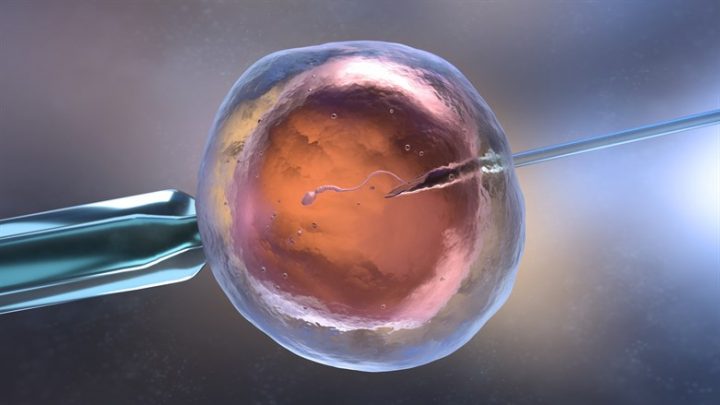
En gran parte del mundo, un número cada vez mayor de mujeres retrasa el parto de su primer hijo hasta los treinta años, e incluso hasta los cuarenta. A esta edad, sus óvulos se están deteriorando rápidamente e, incluso con la fecundación in vitro (FIV), sus perspectivas de concepción están lejos de estar garantizadas.
Revertir ese deterioro es el objetivo final del biólogo molecular Dr. Michael Klutstein, jefe del Laboratorio de Investigación de Cromatina y Envejecimiento en la Facultad de Medicina Dental de la Universidad Hebrea de Jerusalem. Esta posibilidad ahora se ha acercado un paso más con la reciente investigación de su laboratorio, llevada a cabo por la estudiante de doctorado Peera Wasserzug-Pash. en colaboración con médicos del Centro Médico Hadassah y de los hospitales Shaare Zedek. Sus conclusiones se publicaron en Aging Cell.
En los seres humanos, los óvulos comienzan a acumular daños en su material genético cuando una mujer es relativamente joven. A menudo, cuando tiene más de treinta años, sus óvulos han acumulado tanto daño en el ADN que no pueden madurar y ser fertilizados. El equipo del Dr. Klutstein identificó con éxito uno de los procesos de envejecimiento que impiden la maduración exitosa de un óvulo. El más importante de ellos es la pérdida de un óvulo. de los procesos de regulación que normalmente impiden que las partes dañinas del ADN se activen.
En muchos sentidos, es una idea extraña en la que pensar: partes de nuestro ADN contienen secciones de material genético que pueden ser perjudiciales. De hecho, aproximadamente la mitad de nuestro genoma está hecho de secuencias similares a virus o fragmentos de virus, que pueden causar daños considerables al ADN si se permite que se activen a través de la expresión. Esta idea ha sido estudiada ampliamente y fue descubierta por Barbara McClintock, quien recibió el Premio Nobel de 1983 por su trabajo sobre este tema.
Es el proceso de envejecimiento lo que causa la falla del sistema para mantener estos elementos dañinos reprimidos e inactivos. Klutstein y su equipo de la Universidad Hebrea, utilizando óvulos de ratón y humanos, no solo identificaron los detalles de estos procesos, sino que mostraron cómo están interrelacionados y, en última instancia, evitan que un óvulo madure.
Para confirmar sus hallazgos, el equipo utilizó productos químicos que imitan los procesos reales que detienen la represión de secciones del ADN del óvulo y liberan los virus que dañan el ADN. La reproducción artificial de los procesos de envejecimiento permitió al equipo vincular los procesos de pérdida de regulación genómica y la expresión de elementos dañinos en los óvulos envejecidos.
La etapa final de su investigación probó formas de revertir los procesos destructivos de envejecimiento en el trabajo en un óvulo. Si los virus o partes de virus se liberaron y activaron en los óvulos envejecidos, entonces tal vez los medicamentos antivirales podrían prevenir este proceso y el daño resultante.
En su artículo, los investigadores demostraron que los medicamentos antivirales revirtieron el proceso en los óvulos de ratón y regresaron a su antiguo yo juvenil. También ha habido un éxito similar utilizando la manipulación genética para insertar dos genes en el ADN de los óvulos de ratón: los genes implantados producen enzimas que previenen la cadena de eventos que conduce a la activación de las partes dañinas del ADN. “Espero que podamos aumentar la fertilidad entre las mujeres mayores que usan medicamentos antivirales”, compartió Klutstein.
CITATION: Loss of heterochromatin and retrotransposon silencing as determinants in oocyte aging. Peera Wasserzug-Pash, Rachel Rothman, Eli Reich, Lital Zecharyahu, Oshrat Schonberger, Yifat Weiss, Naama Srebnik, Yaara Cohen-Hadad2, Amir Weintraub, Ido Ben-Ami2, Hananel Holzer and Michael Klutstein. Aging Cell, 2022, e13568.
DOI: 10.1111/acel.13568.
FUNDING: Joint Research Fund of the Hebrew University of Jerusalem and Shaare Zedek Medical Center grant, and a Joint Research Fund of the Hebrew University of Jerusalem and Hadassah Medical Center grant. A PhD student fellowship from the Arianne de Rothschild fund and a PhD student fellowship from STEP-GTP.