Utilizando las instalaciones únicas de DESIREE, investigadores de la Universidad de Estocolmo y la Universidad Hebrea de Jerusalem ha sido capaz por primera vez de visualizar directamente los productos neutros de la neutralización mutua del hidronio y el hidróxido, y ha informado de tres canales de productos diferentes: dos canales se atribuyeron a un mecanismo predominante de transferencia de electrones, y un canal más pequeño se asoció con la transferencia de protones. El experimento de colisión de dos haces es un paso importante hacia la comprensión de la dinámica cuántica de esta reacción fundamental. Sus hallazgos se publican en la revista Science.
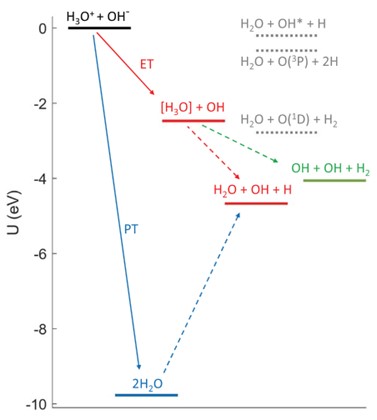
La neutralización mutua (MN) del catión hidronio, H3O+, y el anión hidróxido, OH ̄ para formar moléculas de agua neutras es uno de los procesos químicos más básicos, donde la MN por transferencia de protones (PT) entre los iones hidronio e hidróxido y la reacción inversa de la autoionización del agua, ya que esta gobierna el pH del agua pura. Este proceso ha atraído un interés considerable, pero ha faltado un sondeo experimental directo de los mecanismos de reacción subyacentes. Al darnos cuenta de la interacción en haces fusionados de dos especies iónicas con una velocidad relativa cercana a cero, pudimos visualizar directamente los productos neutros de estas reacciones y observar tres canales de productos diferentes. Dos canales se atribuyen a un mecanismo predominante de transferencia de electrones, y un canal más pequeño se asocia con la transferencia de protones. El experimento de colisión de dos haces es un paso importante hacia la comprensión de la dinámica cuántica de esta reacción fundamental.
Un equipo de científicos dirigido por el profesor Daniel Strasser de la Universidad Hebrea se unió a un equipo dirigido por el Dr. Richard Thomas de la Universidad de Estocolmo, para investigar esta reacción utilizando las instalaciones de DESIREE.
Aquí, los iones de hidronio e hidróxido se crean de forma independiente, se preparan y se permite que interactúen de manera controlada sin que interfieran otras moléculas cercanas. A continuación, se mide la reacción de neutralización mutua mediante la detección de coincidencias de los productos neutros individuales.
En el agua líquida, la transferencia de protones es el único mecanismo de reacción, mientras que, en el sistema aislado, domina la transferencia de electrones y la transferencia de protones es un canal menor, pero aún podría identificarse en DESIREE. “Es emocionante poder observar directamente la competencia entre los mecanismos de transferencia de electrones y protones en esta reacción”, dijo Daniel Strasser. La excitación interna del producto resuelta por el mecanismo informado, así como la energía de colisión y la dependencia inicial de iones y temperatura, proporcionan un punto de referencia para modelar los mecanismos de transferencia de carga en diferentes entornos que contienen “iones de agua”.
“Es fantástico que podamos adoptar un enfoque ascendente para abordar uno de los desafíos más difíciles de la química física”, dijo Richard Thomas. “Esperamos volver a agregar complejidad lentamente al experimento, agregando una molécula de agua a la vez, y estudiando el efecto de esto, ya que, en algún momento, la transferencia de electrones debe disminuir de tal manera que el canal de transferencia de protones domine por completo, y nos gustaría saber cuándo es eso”.
“La instalación de DESIREE fue motivada en gran medida por la capacidad de estudiar la neutralización mutua de iones moleculares, y este es un hito para la instalación que abre una serie de posibilidades para futuros estudios por parte de los usuarios de DESIREE”, dijo el profesor Henning Schmidt, director de la instalación de DESIREE y coautor del artículo.
El artículo de investigación titulado “The mutual neutralization of hydronium and hydroxide”, ya está disponible en Science.
Investigadores
Alon Bogot1, Mathias Poline2, MingChao Ji2, Arnaud Dochain2, Ansgar Simonsson2, Stefan Rosén2, Henning Zettergren2, Henning T. Schmidt2, Richard D. Thomas2, Daniel Strasser1.
Instituciones
1) Instituto de Química, Universidad Hebrea de Jerusalem.
2) Departamento de Física, Universidad de Estocolmo.