Para dar a los tratamientos contra el cáncer la mayor probabilidad posible de éxito, los pacientes a menudo son tratados con múltiples medicamentos que atacan el cáncer utilizando diferentes mecanismos. Un equipo de investigadores ha combinado tres fármacos altamente potentes en un solo profármaco multiobjetivo que se activa en las células tumorales.
Como informa el equipo en la revista Angewandte Chemie International Edition, su profármaco fue más efectivo y causó menos efectos secundarios en ratones, que los medicamentos solos o en una mezcla.
Los tratamientos modernos contra el cáncer toman varias rutas diferentes para combatir el cáncer, a menudo empleando un cóctel de medicamentos para mejorar las posibilidades de éxito. Sin embargo, el cuerpo humano no es adecuado para recibir tantos medicamentos a la vez, y los efectos secundarios desagradables, incluso que alteran la vida, son sinónimos de tratamiento contra el cáncer.
Para reducir la carga en los cuerpos de los pacientes, los equipos de investigación dirigidos por Dan Gibson, de la Universidad Hebrea de Jerusalem, y Victor Brabec de la Academia Checa de Ciencias en Brno, se han unido a una serie de medicamentos contra el cáncer en un solo profármaco. “Cuando se combina en un solo profármaco, solo hay un comportamiento farmacocinético y un perfil de toxicidad diferente”, dice Gibson.
Los tres medicamentos elegidos por el equipo, gemcitabina, oxaliplatino y doxorrubicina, son todos medicamentos probados contra el cáncer. Los medicamentos funcionan dañando el ADN de las células cancerosas utilizando diferentes mecanismos, evitando que las células se reproduzcan y, además, estimulando la propia respuesta inmune del paciente para atacar las células cancerosas. “Nuestro objetivo es preparar profármacos a base de platino que liberen dos o tres medicamentos aprobados por la FDA que se usan juntos para tratar una indicación determinada”, dice Gibson.
Se utilizaron dos tipos de enlazadores autoinmolativos para vincular el oxaliplatino que contiene platino con los otros profármacos orgánicos, donde “autoinmolativo” significa que los enlazadores se autodestruirán en las condiciones adecuadas. Los tipos de enlazadores seleccionados del profármaco multiobjetivo se desglosaron para activar los fármacos mediante el entorno reductor que se encuentra en las células tumorales.
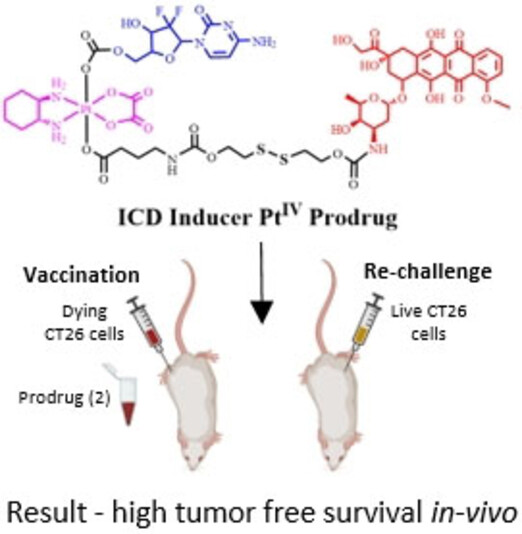
En modelos celulares y animales, el fármaco combinado del equipo demostró ser considerablemente más efectivo que los medicamentos solos o en una mezcla. Los efectos secundarios también se redujeron, con una mayor selectividad para las células cancerosas, lo que significa que las células menos sanas se dañaron.
El equipo cree que una gran parte de este éxito se debió a los enlazadores que utilizaron en su profármaco multitargeting.
“La impresionante actividad biológica se puede atribuir al diseño adecuado de los enlazadores autoinmolantes que conectan los tres fármacos que facilitan la liberación de los fármacos en su forma activa, explotando así las mejores propiedades de los fármacos individuales”, afirmaron.
Más información: Amrita Sarkar et al, Multitargeting Prodrugs that Release Oxaliplatin, Doxorubicin and Gemcitabine are Potent Inhibitors of Tumor Growth and Effective Inducters of Immunogenic Cell Death, Angewandte Chemie International Edition (2023). DOI: 10.1002/anie.202310774
Fuente: MedicalXpress


